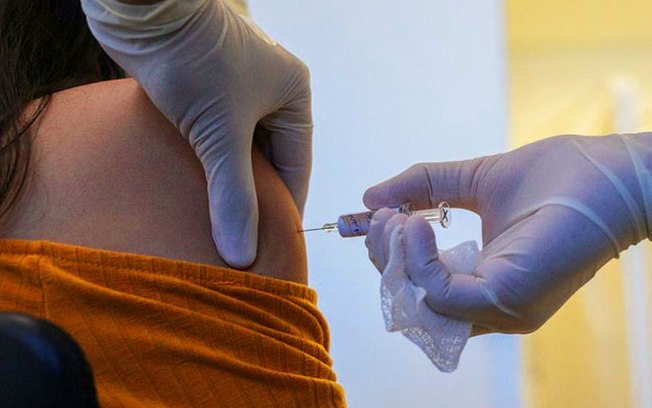
Na semana passada, o instituto revelou que a vacina tinha 78% de proteção para casos leves e moderados da covid-19. Dados cumprem critérios da OMS
A vacina contra a covid-19 desenvolvida pelo laboratório chinês Sinovac em parceria com o Instituto Butantan tem uma taxa de eficácia global de 50,38%. A eficácia global é a capacidade de redução de riscos de contrair a doença se receber a vacina. O dado foi apresentado nesta terça-feira (12), após a divulgação de um recorte da pesquisa dividir a comunidade científica brasileira. Os dados de eficácia global ―mais baixos que os de eficácia sobre casos leves e graves da doença, mas dentro dos parâmetros estabelecidos pela Organização Mundial da Saúde― não põem em xeque a capacidade da vacina de proteger contra a covid-19. Como já haviam anunciado as autoridades de saúde paulistas, a Coronavac tem se mostrado eficaz para prevenir casos que precisam de hospitalização e mortes por covid-19 e, portanto, deve ter impacto em frear pandemia no Brasil, que já contabiliza mais de 203.000 óbitos e vê as infecções voltarem a subir em várias regiões e pressionar sistemas de saúde.
Na semana passada, o Governo de São Paulo e o Instituto Butantan anunciaram que a Coronavac tinha 78% de proteção para casos leves e moderados e 100% de proteção contra casos graves da doença. Isso significa que os que receberam as duas doses do imunizante criaram anticorpos contra o novo coronavírus e, mesmo os contaminados, tiveram apenas sintomas leves. Os 50,38% do resultado geral estão abaixo dos dados de mais de 90% de eficácia de imunizantes que usam uma tecnologia diferente, de RNA mensageiro, considerado por cientistas o futuro da imunização, mas que neste momento as vacinas desenvolvidas requerem uma logística mais complicada de armazenamento. Seja como for, há problemas em uma comparação estrita desse dado neste sentido pela divergência dos estudos. Assim como vacinas contra diferentes doenças. Mesmo assim, essa questão foi mencionada na coletiva. Vacinas com eficácia entre 60% e 70% controlam surtos de gripe e tuberculose. “São dados absolutamente similares às vacinas de rotavírus e coqueluche (…) e acho que é inequívoco o impacto dessas vacinas na vida da população”, destacou Marcelo Aurelio Safadi, presidente do Departamento de Infectologia da Sociedade Brasileira de Pediatria, para exemplificar o impacto de vacinas com dados globais menores.
O diretor do centro de segurança clínica e farmacovigilância do Butantan, Alex Precioso, salientou que o perfil de segurança da Coronavac tem se mantido desde o início do estudo. Foram observadas apenas reações leves, como dor no local da injeção, dor de cabeça, fadiga, cansaço e mialgia, sem diferença entre as faixas etárias estudadas. “Foram eventos leves que não interferiram com as atividades diárias dos participantes”, pontua. Ele diz que também não houve registro nenhum efeito adverso grave associado à vacina e que, em termos de reações alérgicas, a frequência foi baixa, de 0,3% e sem diferenças entre aqueles que receberam a vacina o placebo.
“Temos uma vacina eficaz”, afirma o diretor médico de pesquisa clínica do Butantan, Ricardo Palácios. A vacina pode ter então um papel importante para reduzir as hospitalizações e começar a desafogar o sistema de saúde brasileiro, que já colapsou em algumas regiões do país. Ter um percentual de eficácia global mais baixo significa que uma fatia maior da população precisará receber o imunizante para chegar a uma imunidade de rebanho e conseguir diminuir de fato a transmissão do vírus. Na segunda-feira, a Indonésia aprovou uso emergencial da Coronavac e anunciou uma eficácia de 65,3% no ensaio local, mas cientistas apontam a dificuldade de comparar o percentual com o brasileiro, já que as pesquisas têm número de voluntários distintos e mesmo diferenças sobre, por exemplo, o que é considerado um evento grave. O Butantan diz ter usado uma definição de caso muito abrangente.
O debate criado em torno da transparência de divulgação dos resultados da pesquisa da Coronavac no Brasil ―que envolveu quase 13.000 voluntários desde julho― ocorreu porque foi anunciado apenas um recorte dos dados, sem a informação geral normalmente anunciada pelos laboratórios e instituições responsáveis pelos imunizantes. Isso dividiu a comunidade científica brasileira e gerou receio de dificultar o convencimento da população para receber a Coronavac, imunizante alçado ao centro da disputa política e ideológica entre os ex-aliados João Dória e Jair Bolsonaro. O governador de São Paulo e o presidente do Brasil têm encampado uma verdadeira corrida pelos louros públicos do primeiro imunizante a ser disponibilizado no país, o que vem jogando pressão sobre a Anvisa, agência brasileira responsável por autorizar o uso emergencial das vacinas.
A Anvisa recebeu a solicitação para uso emergencial de 6 milhões de doses da Coronavac e 2 milhões de doses da vacina da Astrazeneca, a aposta federal por meio da Fiocruz. Mas pediu mais informações sobre o imunizante do Instituto Butantan, consideradas razoáveis por pesquisadores. No momento, a agência corre contra o tempo para analisar todos os dados e pede informações complementares na tentativa de analisá-los no apertado prazo de dez dias, contados a partir de 8 de janeiro. Por enquanto, estas 8 milhões de doses representam o quantitativo de vacinas para começar a vacinação no Brasil. O Governo Federal também negocia a aquisição do imunizante da Pfizer, que exige uma logística de armazenamento mais complexa. O laboratório teve uma reunião com a Anvisa nesta terça-feira (12) para esclarecimentos sobre o processo de solicitação do uso emergencial, mas não houve definição de uma possível data para isso.
Início da campanha nacional ainda é uma incógnita
Ainda é uma incógnita quando o Brasil deverá de fato começar a vacinação. O Governo de São Paulo tem mantido uma previsão para o dia 25 de janeiro, mas depende de como avança o processo da Coronavac na Anvisa, que tem pedido dados adicionais não apresentados. Segundo um painel da própria Anvisa, faltam 5% da documentação necessária e 37% está pendente de complementação. Já a da AstraZeneca tem cerca de 5% da documentação pendente de complementação. Este imunizante também enfrentou críticas de falta de transparência ao divulgar uma eficácia de cerca de 70%, a partir de uma análise combinada entre duas doses (62% de eficácia) e uma dose e meia aplicada por erro em um determinado grupo de voluntários (que superou 90% de eficácia). A vacina da AstraZeneca foi testada em voluntários brasileiros sob a coordenação da Unifesp, que diz que “os resultados são divulgados pela AstraZeneca e Oxford, a Unifesp não divulga dados, já que é apenas um braço do estudo”. Assim, não houve divulgação apenas do braço brasileiro do estudo.
Sob pressão de governadores e secretários da Saúde, o Governo Federal estima começar a vacinação ainda em janeiro, no melhor cenário, ou início de março, no pior deles. Na segunda-feira (12), o ministro da Saúde, Eduardo Pazuello, chegou a dizer que a imunização começará no “Dia D e na hora H”. “Todos os estados receberão simultaneamente as vacinas, no mesmo dia. A vacina vai começar no dia D, na hora H, no Brasil. No primeiro dia que a autorização for feita, a partir do terceiro ou quarto dia estará nos Estados e municípios para iniciar a vacinação. A prioridade já está dada, é o Brasil todo. Vamos fazer como exemplo para o mundo. Os grupos prioritários já estão distribuídos”, afirmou.
Nos últimos dias, o Brasil deu um passo importante para iniciar a vacinação com as solicitações dos dois primeiros imunizantes para uso emergencial, mas ainda enfrenta problemas com o baixo quantitativo de doses no horizonte e há poucas informações públicas sobre como será o rateio entre os Estados. É neste contexto que Pazuello tem ventilado a possibilidade de dar uma única dose da vacina para imunizar um quantitativo maior de pessoas ― uma estratégia discutida em outros países, mas sem respaldo científico, já que as pesquisas da maioria dos imunizantes foram desenhadas com a aplicação de duas doses.
A biomédica Mellanie Fontes-Dutra afirma que é bastante complicado e requer cautela ao levantar a possibilidade de adaptar e aplicar uma única dose, se não há estudos específicos. “O que está sendo discutido em alguns países é espaçar até 12 semanas de uma dose pra outra, para vacinar muita gente e depois vir com uma segunda dose porque após a primeira os dados já apontam para uma imunização que pode ser interessante, dependendo da estratégia adotada nas campanhas e vacinação. Uma modificação do protocolo vai requerer mais estudos para respaldar isso”, pondera.
A Organização Mundial da Saúde (OMS) indicou na última segunda-feira que o mundo não deve ter imunidade de rebanho neste ano de 2021 diante das limitações para produzir um quantitativo de doses suficientes das mais diversas vacinas. Enquanto isso, é preciso seguir as medidas de prevenção, como uso de máscaras e distanciamento social.
Fonte: El País




